Foto: Anadolu
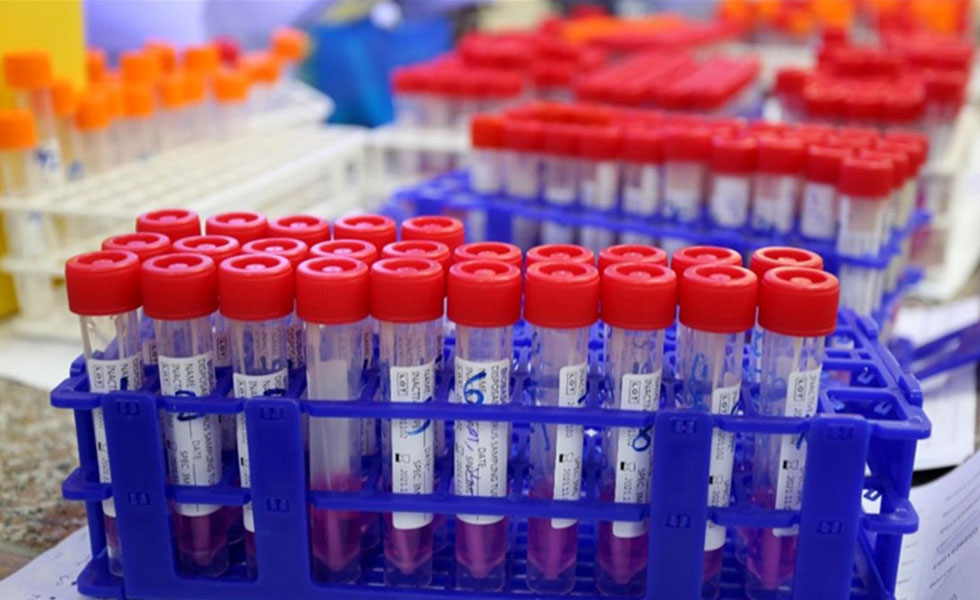
La Administración de Medicamentos y Alimentos de los Estados Unidos (FDA, por su sigla en inglés) informó este en un comunicado que ha decidido conceder la autorización de emergencia para el uso de Ellume COVID-19 Home, la primera prueba casera para detectar el nuevo coronavirus.
“La autorización de hoy es un hito importante en las pruebas de diagnóstico para COVID-19. Al autorizar una prueba para su uso sin autorización médica, la FDA permite que se venda en lugares como farmacias, donde un paciente puede comprarla, hisoparse la nariz, ejecutar la prueba y conocer los resultados en tan solo 20 minutos”, dijo el comisionado de la FDA, Stephen Hahn.
De acuerdo con la FDA esta prueba casera pudo identificar inequívocamente el 100% de las muestras negativas y el 96% de las muestras positivas en personas con síntomas. En personas asintomáticas la prueba identificó correctamente el 96% de las negativas y el 91% de las muestras positivas.
“La prueba casera Ellume COVID-19 utiliza un analizador que se conecta con una aplicación de software en un teléfono inteligente para ayudar a los usuarios a realizar la prueba e interpretar los resultados. Los resultados se entregan en tan solo 20 minutos a las personas a través de sus teléfonos inteligentes”, dijo la FDA.
La aplicación móvil informa los resultados según corresponda a las autoridades de salud pública para monitorear la prevalencia de la enfermedad.
Ellume COVID-19 Home es una prueba de antígeno cuyo precio de venta al público sería de USD 30, según sus fabricantes. La compañia espera que para enero de 2021 se produzcan aproximadamente tres millones de pruebas.